-
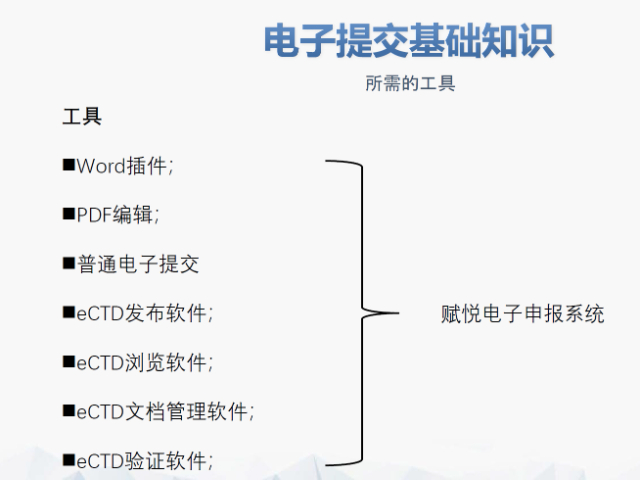 山東賦悅科技eCTD服務商
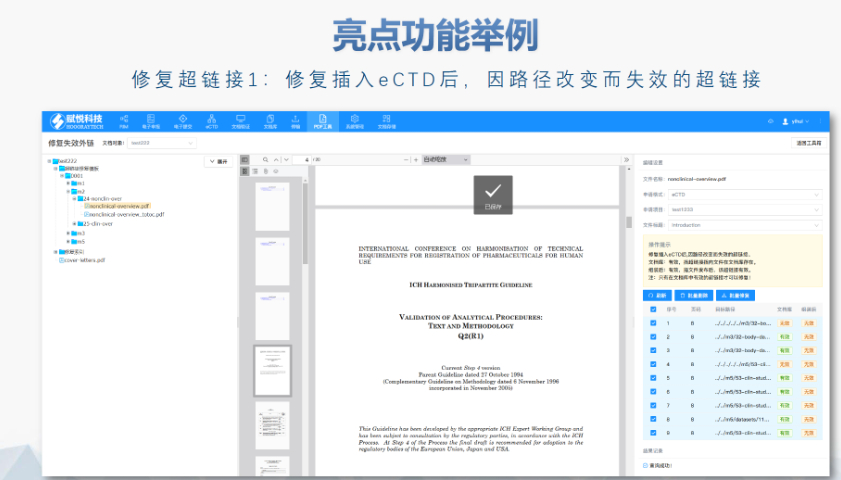
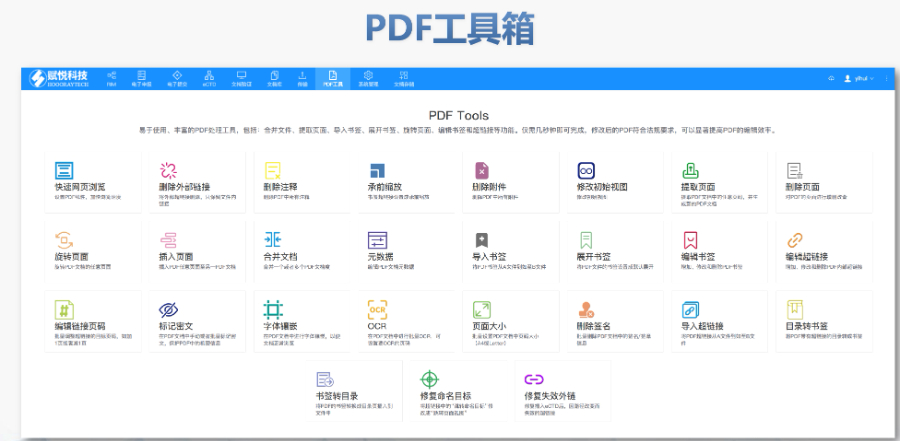
山東賦悅科技eCTD服務商PDF工具箱 ?批量處理與格式修復 支持PDF合并、拆分、提取頁面、旋轉頁面等操作,可批量修復字體未嵌入、超鏈接錯誤等問題,確保文件符合藥品注冊法規要求。 ?智能書簽與超鏈接管理 提供書簽導入/導出、超鏈接自動生成(支持關鍵字搜索定位鏈接)、題注超鏈接拖拽式編...
2025-04-01 -
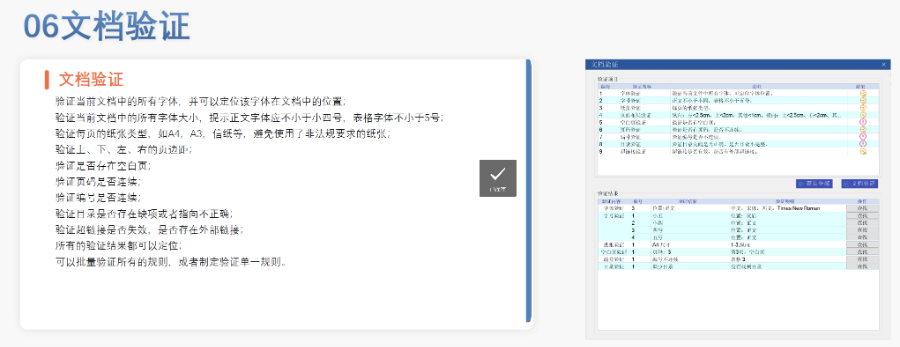 合肥國內注冊eCTD歡迎選購
合肥國內注冊eCTD歡迎選購GDUFA III框架與費用分類 2022年更的GDUFA III將費用分為ANDA申請費、DMF認證費、項目費及設施費四類,實施周期至2027年。2025財年ANDA費用漲至約22萬美元,較2024年增幅達27.5%,反映審評成本上升。 ?ANDA申請費規則...
2025-04-01 -
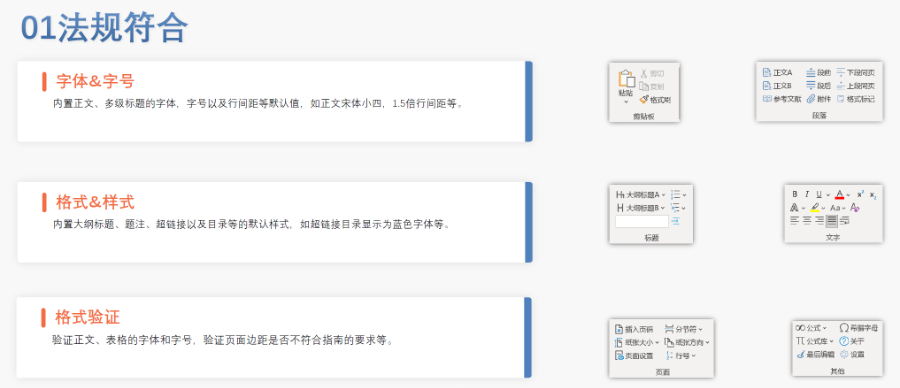 南京生物制品eCTD推薦
南京生物制品eCTD推薦歐洲藥品管理局:集中審評程序由歐洲藥品管理局(European Medicines Agency, EMA)負責協調。 人用藥品委員會:人用藥品委員會(Committee for Medicinal Products for Human Use, CHMP)負...
2025-04-01 -
 太倉藥品注冊eCTD服務價格
太倉藥品注冊eCTD服務價格DMF維護與合規 ?年度更 即使無變更,每年需提交聲明;重大工藝/設施變更需及時通知客戶并更文件。 ?現場檢查 原料藥企業需通過FDA現場檢查,驗證是否符合ICH Q7 GMP標準,并與DMF內容一致。 ?轉讓與關閉 ?轉讓:需書面通知FDA并提供持有者信息。...
2025-03-31 -
 楊浦區國產eCTD性價比高
楊浦區國產eCTD性價比高審評效率與時間線優化 eCTD的標準化縮短了審評周期:集中程序平均審評時間從18個月降至12個月,互認程序可在90天內完成成員國意見協調。自動化驗證工具減少了格式錯誤導致的退審率,但復雜藥學數據的科學審評仍需較長時間。申請人可通過預提交會議(Pre-submi...
2025-03-31 -
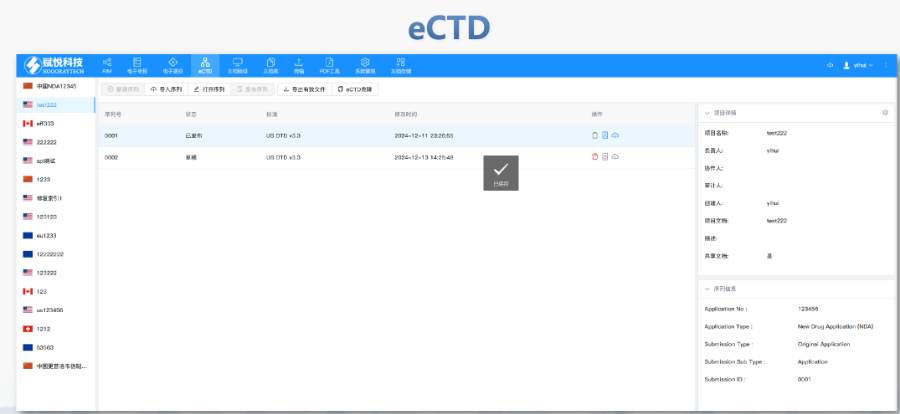 蕪湖生物制品eCTD系統
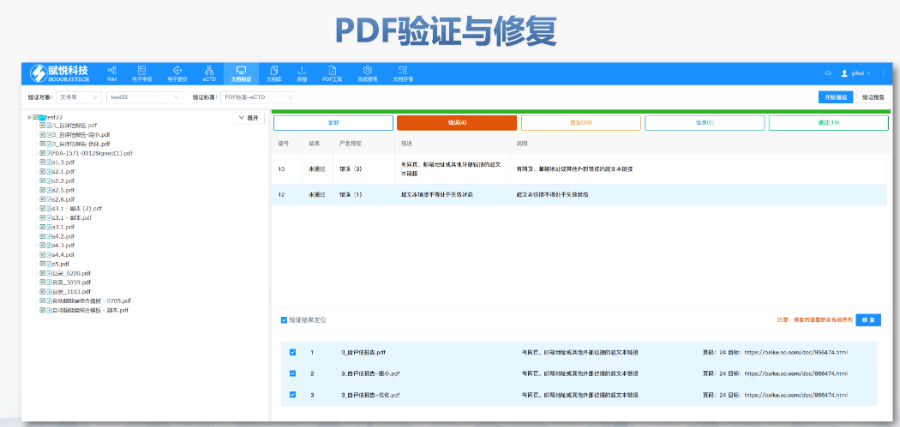
蕪湖生物制品eCTD系統美國eCTD驗證采用三級分類:“錯誤”(必須修正)、“警告”(建議修正)、“提示信息”(參考)。例如,PDF文件版本不符或加密保護屬于“錯誤”,而書簽路徑非相對性則可能列為“警告”。驗證失敗將直接導致退審,企業需通過LORENZ Validator等工具預檢,...
2025-03-31 -
 海南eCTD服務價格
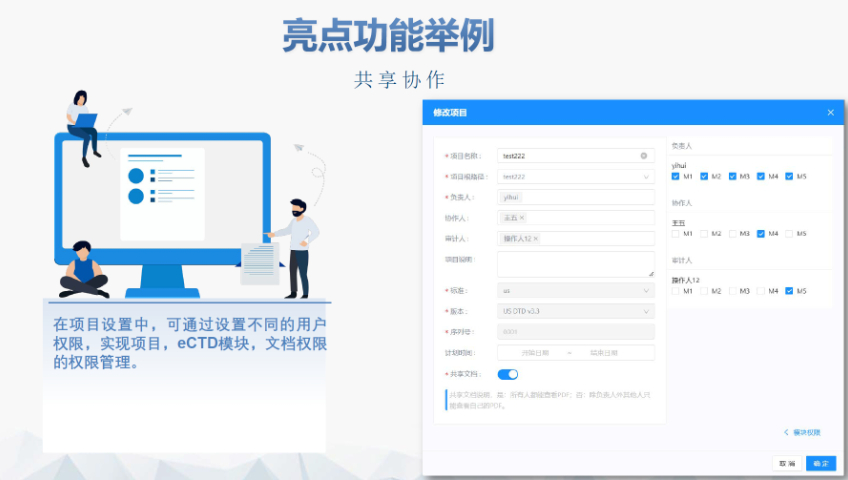
海南eCTD服務價格eCTD提交流程與ESG系統:FDA要求通過電子提交網關(ESG)傳輸eCTD文件,單個文件大小限制為10GB,超限需拆分或通過物理介質(如光盤)遞交。提交前需預分配申請號(如NDA編號),并通過ESG測試賬戶驗證技術合規性。序列號命名規則為4位數字(如000...
2025-03-31 -
 吳江區電子申報eCTD服務商
吳江區電子申報eCTD服務商緊急申報與特殊通道:FDA設置緊急申報通道(如Pre-EUA和EUA),允許在公共衛生事件中快速提交資料。此類申請需在模塊1.19注明特殊標識,并通過ESG加急處理。 eCTD版本兼容性與過渡策略:eCTD 4.0支持向前兼容,允許v3.2.2文件無縫過渡。企...
2025-03-31 -
 合肥原料藥eCTD歡迎選購
合肥原料藥eCTD歡迎選購歐洲藥品管理局:集中審評程序由歐洲藥品管理局(European Medicines Agency, EMA)負責協調。 人用藥品委員會:人用藥品委員會(Committee for Medicinal Products for Human Use, CHMP)負...
2025-03-30 -
 太倉藥品注冊eCTD系統
太倉藥品注冊eCTD系統eCTD的實施為監管機構和企業帶來了多重機遇。電子化申報資料能夠極大地加速審評效率,減少人為判斷錯誤和數據混淆的情況,從而提高審評的準確性和速度。同時,eCTD帶來的數據標準化機遇使得全球監管機構的資料內容和電子格式得以統一,有助于在不同監管機構之間進行數據傳...
2025-03-30 -
 上海國際注冊eCTD是什么
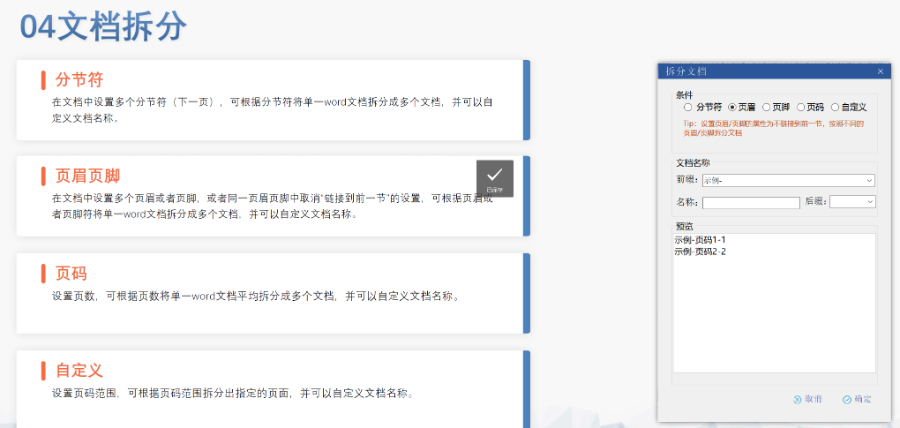
上海國際注冊eCTD是什么賦悅eCTD系統 ?文件驗證與修復 支持自動驗證文件格式(如PDF屬性、字體嵌入、超鏈接完整性等),并一鍵修復不符合法規要求的文件。例如,系統會自動檢查XML主干文件的結構合規性,確保符合中國、美國、歐盟等地區的eCTD法規標準。 ?eCTD組裝與發布 可自動...
2025-03-30 -
 浙江eCTD供應商
浙江eCTD供應商申報流程與要求 ?資料準備 ?內容要求:包括產品描述、生產工藝(原材料來源、設備參數等)、質量控制標準(SOP、穩定性數據)、安全性與毒性研究等。 ?格式規范: 采用CTD(通用技術文件)格式,按模塊分章節(如模塊3為CMC數據)。 電子提交需符合eCTD標準...
2025-03-30 -
 南京國際注冊eCTD格式
南京國際注冊eCTD格式澳大利亞的藥品電子通用技術文檔(eCTD)注冊申報體系是澳大利亞y藥品商品管理局(TGA)推動藥品審評現代化的重要舉措。eCTD作為國際通行的電子化注冊申報標準,通過結構化數據格式(如XML)整合了藥品質量、安全性和有效性的技術文檔,實現了從傳統紙質遞交向數字...
2025-03-30 -
 蕪湖NDAeCTD銷售電話
蕪湖NDAeCTD銷售電話美國藥物主文件(Drug Master File, DMF)是向FDA提交的機密技術文件,用于支持藥品生產、質量控制及合規性審查。以下為申報的要點和流程總結: DMF概述與類型 ?定義與作用 DMF是藥品生產全過程的詳細檔案,包含原料藥、輔料、包裝材料等的生產...
2025-03-29 -
 瑞士eCTD
瑞士eCTD美國eCTD的強制實施時間與范圍:美國自2017年5月5日起要求藥申請(NDA)、仿制藥申請(ANDA)和生物制品許可申請(BLA)必須通過eCTD格式提交,2018年5月5日進一步擴展至臨床試驗申請(IND)和藥品主文件(DMF)。FDA通過《聯邦食品、藥品...
2025-03-29 -
 安徽國際注冊eCTD找哪家
安徽國際注冊eCTD找哪家緊急申報與特殊通道:FDA設置緊急申報通道(如Pre-EUA和EUA),允許在公共衛生事件中快速提交資料。此類申請需在模塊1.19注明特殊標識,并通過ESG加急處理。 eCTD版本兼容性與過渡策略:eCTD 4.0支持向前兼容,允許v3.2.2文件無縫過渡。企...
2025-03-29 -
 上海新藥eCTD發布系統
上海新藥eCTD發布系統經濟影響與成本效益 盡管初期投入較高(平均每企業需50萬歐元),但eCTD可減少30%的審評延遲成本,長期效益。仿制藥企業通過eCTD復用原研數據,節省80%的申報準備時間。歐盟預算撥款2億歐元資助中小企業完成數字化轉型。 倫理審查與數據隱私 eCTD中的患者...
2025-03-29 -
 寧波原料藥eCTD軟件
寧波原料藥eCTD軟件eCTD生命周期管理與變更提交:歐盟要求eCTD申報資料覆蓋藥品全生命周期,包括提交、補充申請及實質性變更。例如,增成員國需提交“附加成員國序列”,審評時間約52-83天;重大變更(如生產工藝調整)需創建序列并通過CTIS平臺更模塊3和模塊1的GMP證明。技術...
2025-03-29 -
 閔行區賦悅科技eCTD軟件
閔行區賦悅科技eCTD軟件此次eCTD實施范圍的擴大對外企而言影響。實施范圍的擴大為外企提供了更多選擇,特別是在產品線中NDA和AND占比相當的情況下。外企的系統和流程相對成熟,因此它們對eCTD擴大范圍持積極態度,更愿意嘗試和改變。盡管過程中可能遇到技術或法規上的問題,但企業認為通過...
2025-03-29 -
 山東藥品注冊eCTD推薦
山東藥品注冊eCTD推薦eCTD生命周期管理與變更提交:歐盟要求eCTD申報資料覆蓋藥品全生命周期,包括提交、補充申請及實質性變更。例如,增成員國需提交“附加成員國序列”,審評時間約52-83天;重大變更(如生產工藝調整)需創建序列并通過CTIS平臺更模塊3和模塊1的GMP證明。技術...
2025-03-29 -
 工業園區eCTD性價比高
工業園區eCTD性價比高美國電子提交通道ESG(Electronic Submissions Gateway)是美國食品藥品監督管理局(FDA)建立的電子化監管信息提交系統,旨在為制藥、生物制品、醫療器械等行業提供安全、高效的電子申報服務。自2006年啟用以來,ESG已成為FDA接收...
2025-03-29 -
 杭州新藥eCTD名稱
杭州新藥eCTD名稱此次eCTD實施范圍的擴大對外企而言影響。實施范圍的擴大為外企提供了更多選擇,特別是在產品線中NDA和AND占比相當的情況下。外企的系統和流程相對成熟,因此它們對eCTD擴大范圍持積極態度,更愿意嘗試和改變。盡管過程中可能遇到技術或法規上的問題,但企業認為通過...
2025-03-29 -
 工業園區生物制品eCTD格式
工業園區生物制品eCTD格式美國于2003年成為全球早采用eCTD(電子通用技術文檔)的國家之一,初由CDER和CBER作為電子提交平臺試點。2008年起,eCTD正式成為藥申請(NDA)和生物制品許可申請(BLA)的標準格式,并在2012年通過《藥申報者付費法案》(PDUFA)進一步強...
2025-03-29 -
 工業園區賦悅科技eCTD品牌
工業園區賦悅科技eCTD品牌技術壁壘與興市場挑戰 非洲和東南亞國家逐步采納eCTD,但其IT基礎設施薄弱導致實施進度滯后。歐盟通過“eCTD全球化倡議”提供技術援助,幫助興市場建立驗證體系和培訓中心。跨國藥企需針對不同區域定制遞交策略,例如在模塊1附加本地穩定性數據。 監管科學與創激勵 ...
2025-03-29 -
 安徽新藥eCTD常用解決方案
安徽新藥eCTD常用解決方案美國于2003年成為全球早采用eCTD(電子通用技術文檔)的國家之一,初由CDER和CBER作為電子提交平臺試點。2008年起,eCTD正式成為藥申請(NDA)和生物制品許可申請(BLA)的標準格式,并在2012年通過《藥申報者付費法案》(PDUFA)進一步強...
2025-03-29 -
 吳江區原料藥eCTD歡迎選購
吳江區原料藥eCTD歡迎選購技術壁壘與興市場挑戰 非洲和東南亞國家逐步采納eCTD,但其IT基礎設施薄弱導致實施進度滯后。歐盟通過“eCTD全球化倡議”提供技術援助,幫助興市場建立驗證體系和培訓中心。跨國藥企需針對不同區域定制遞交策略,例如在模塊1附加本地穩定性數據。 監管科學與創激勵 ...
2025-03-29 -
 貴州瑞士eCTD
貴州瑞士eCTD從紙質到電子的歷史過渡 2017年前,美國允許紙質與eCTD并行提交,但此后逐步淘汰紙質通道,保留緊急情況下的例外審批。2020年電子化后,所有IND、NDA、ANDA和DMF強制采用eCTD格式。 ?系統平臺升級 FDA通過“藥品業務應用系統”和“藥品eCT...
2025-03-28 -
 上海仿制藥eCTD銷售電話
上海仿制藥eCTD銷售電話美國于2003年成為全球早采用eCTD(電子通用技術文檔)的國家之一,初由CDER和CBER作為電子提交平臺試點。2008年起,eCTD正式成為藥申請(NDA)和生物制品許可申請(BLA)的標準格式,并在2012年通過《藥申報者付費法案》(PDUFA)進一步強...
2025-03-28 -
 貴州國內注冊eCTD
貴州國內注冊eCTD從紙質到電子的歷史過渡 2017年前,美國允許紙質與eCTD并行提交,但此后逐步淘汰紙質通道,保留緊急情況下的例外審批。2020年電子化后,所有IND、NDA、ANDA和DMF強制采用eCTD格式。 ?系統平臺升級 FDA通過“藥品業務應用系統”和“藥品eCT...
2025-03-28 -
 安徽化學藥品eCTD注冊系統
安徽化學藥品eCTD注冊系統eCTD生命周期管理與變更提交:歐盟要求eCTD申報資料覆蓋藥品全生命周期,包括提交、補充申請及實質性變更。例如,增成員國需提交“附加成員國序列”,審評時間約52-83天;重大變更(如生產工藝調整)需創建序列并通過CTIS平臺更模塊3和模塊1的GMP證明。技術...
2025-03-28